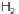Geoscience Reference
In-Depth Information
3
Abb. 64:
Prädominanz-(Stabilitäts-)
felder für Eisen II- und III-Spezies für
Aktivitäten von 0,01 mg bis 100 mg
gelöstes Eisen/kg (nach H
EM
, 1961).
Abb. 63 zeigt die Stabilitätsgrenzen des Wassers
sowie häufig vorkommende
E
H
/pH-Verhältnisse
natürlicher Wässer.
E
H
/pH-Diagramme
geben also die Bereiche
der in den verschiedenen Oxidations-pH-Stufen
vorherrschenden gelösten Ionen und Verbindun-
gen der Elemente an. In Abb. 64 sind z.B. die Prä-
dominanz-(Stabilitäts-)felder der verschiedenen
Eisen-Spezies unter Normalbedingungen (
T
=
298 K,
p
= 10
5
Pa, unterschiedliche Ionenaktivitä-
ten) dargestellt. Die Prädominanzfelder der je-
weiligen Spezies werden durch die Stabilitäts-
grenzen eingegrenzt, an deren Linien die Aktivi-
täten der angrenzenden Ionen gleich groß sind.
Waagerecht verlaufende Grenzlinien (z.B. von
Fe
3+
in der linken oberen Ecke) kennzeichnen
pH-unabhängige Redoxreaktionen, an denen nur
Elektronen, jedoch keine H
+
- oder OH
-
-Ionen
beteiligt sind; sie sind daher nur
E
H
-abhängig.
Senkrecht verlaufende Grenzlinien werden durch
H
+
- oder OH
-
-Ionen bestimmt, es tritt kein Elek-
tronenübergang auf, sie sind also pH-abhängig.
Schräg verlaufende Stabilitätsgrenzen geben pH-
und
E
H
-abhängige Spezies wieder. Außerhalb der
Prädominanzfelder sind die jeweiligen Spezies
nur untergeordnet oder gar nicht (wie z.B. H
2
O
mit den gasförmigen Anteilen H
2
und O
2
) exis-
tent. Eine umfangreiche Zusammenstellung von
Prädominanzfeldern findet sich bei H
EM
(1961)
und S
EEBURGER
& K
Äß
(1989).
Außer dem Redoxpotenzial wird häufig der
sog.
rH-Wert
ermittelt. Dieser ist ein pH-Wert-
unabhängiges Maß für das Redoxvermögen eines
Systems. Der rH-Wert ist als der negative dekadi-
sche Logarithmus des Wasserstoff-Partialdrucks
(also rH = -lg
p
p
(H
2
)) definiert, mit dem eine
Platinelektrode beladen sein müsste, um eine der
Lösung entsprechende Reduktionswirkung aus-
zuüben.
Wie oben angeführt, gilt im reduzierenden Be-
reich
2 H
+
+ 2 e
-
,
H
2
→