Geoscience Reference
In-Depth Information
@
@
U
U
@
G
.
T
;
p
/ D
U
V
S
D
U
C
pV
TS
@
V
S
S
V
„ ƒ‚ …
„ ƒ‚ …
T
p
dG
.
T
;
p
/ D
T
dS
pdV
„ ƒ‚ …
dU
.
S
;
V
/
C
pdV
C
Vdp
TdS
SdT
D
SdT
C
Vdp
:
(7.4)
Da Änderungen der gibbsschen Energie Prozesse antreiben,
ist sie von besonderem Interesse in der globalen Geophysik.
Es sind auch Übergänge mit dem Austausch nur einer Va-
riablen möglich. So gilt beispielsweise für den Übergang von
der inneren Energie U
.
S
;
V
/
zur freien Helmholtz-Energie
F
.
T
;
V
/
in Abwesenheit chemischer Reaktionen:
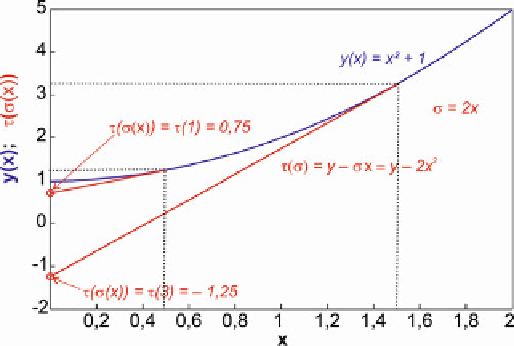
Abb. 7.1
Die Legendre-Transformierte der punktweise vorgegebenen
Funktion y D x
2
C
1
(
blaue Kurve
) mit der Steigung
¢
D
2
xistdie
Menge der durch die Tangenten
£.¢/
D y
2
x
2
(
rote Geraden
) und
zugehörigen Y-Achsenabschnitte definierten Punkte (
rote Kreise
)
@
U
@
S
F
.
T
;
V
/ D
U
S
D
U
TS
V
„ ƒ‚ …
T
(7.5)
dF
.
T
;
V
/ D
T
dS
pdV
„ ƒ‚ …
dU
TdS
SdT
erläutert und danach auf Funktionen zweier Veränderlicher
übertragen werden.
Ist y
.
x
/
eine Funktion von x, dann ist
¢ D
dy
=
dx die Stei-
gung ihrer Tangente
.
S
;
V
/
D
SdT
pdV
;
am Punkt x, welche die y-Achse im
ist
£.¢/ D
y
.
x
/
x
¢
. Diese Gleichung definiert die durch
y beschriebene Kurve als die Einhüllende ihrer Tangenten
£
.
Allgemein gilt diese Definition auch mit umgekehrtem Vor-
zeichen:
£.¢/ D
x
¢
y
.
x
/
, in der Thermodynamik wird
jedoch üblicherweise die erste Vorzeichenkonvention ver-
wendet.
Im zweidimensionalen Fall wird, analog zum eindimen-
sionalen Fall, eine als Funktion f
.
x
;
y
/
zweier Variablen defi-
nierte Fläche als Einhüllende ihrer Tangentenebenen
£.¢; ¦/
dargestellt:
£
Und für den Übergang von der inneren Energie U
.
S
;
V
/
zur
Enthalpie H
.
S
;
p
/
:
@
U
@
V
H
.
S
;
p
/ D
U
V
D
U
C
pV
S
„ ƒ‚ …
p
(7.6)
dH
.
S
;
p
/ D
T
dS
pdV
„ ƒ‚ …
dU
C
pdV
C
Vdp
.
S
;
V
/
D
TdS
C
Vdp
:
Da die Enthalpie ein Maß für die mechanische und nicht-
mechanische Arbeit ist, die ein System zu leisten vermag,
ist sie von praktischer Bedeutung insbesondere in Hinsicht
auf die Gewinnung von Erdwärme und deren Wandlung in
elektrische Energie.
und
6.3
aufgeführten thermodynamischen Zustandsfunktio-
nen und die gibbsschen Fundamentalgleichungen der Ther-
modynamik. Im Falle chemischer Reaktionen treten noch die
Terme
P
i
dn
i
hinzu, wobei
i
die chemischen Potenziale
sind und n
i
die zugehörigen Stoffmengen.
@
f
.
x
;
y
/
@
x
@
f
.
x
;
y
/
@
y
£.¢; ¦/ D
f
.
x
;
y
/
x
y
:
(7.3)
y
x
Damit kann die Legendre-Transformation zur Ableitung der
thermodynamischen Potenziale aus den gibbsschen Funda-
det werden bzw. zum Übergang zwischen den thermodyna-
inneren Energie U
.
S
;
V
/
D
TS
p V zur Gibbs-Energie
G
.
T
;
p
/
gilt somit: